多克隆抗體的制備以及佐劑在其制備中的應用
一、抗體
抗體是地球生命進化史上一類不尋常的蛋白質,是生物醫學界的 “魔力子彈”,在哺乳動物中,抗體能對機體固有的免疫系統起到增強和補充作用,當機體遭遇外界刺激(如細菌、病毒或其他病原微生物等)時,會產生獲得性免疫反應,合成并分泌抗體。
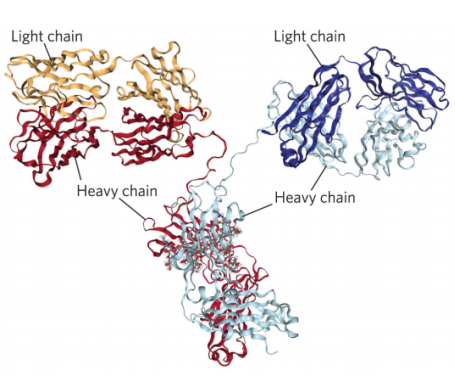
抗體是宿主蛋白質,在體內存在外來分子時產生,它們主要由漿細胞合成,漿細胞是B淋巴細胞譜系中終分化的細胞,并在血液和淋巴中循環,與外來抗原結合。隨后,抗體-抗原復合物主要通過巨噬細胞的吞噬作用從循環中移除。抗體具有重要的結構和功能特征,在功能上,能夠結合抗原和免疫系統的特定細胞或蛋白質,在結構上,抗體由一個或多個“Y”形組成,每個“Y”含有四種多肽,兩種相同的重鏈多肽和兩種相同的輕鏈多肽。根據“Y”型的數量和它們包含的重鏈多肽的類型分為五類,即IgG、IgM、IgA、IgE和IgD,其中IgG在血清中的含量豐富。
二、多克隆抗體
由于抗原分子具有多種抗原決定簇,每一種決定簇可激活具有相應抗原受體的B細胞產生免疫應答,因而可產生多種針對不同抗原決定簇的抗體,這些由不同B細胞克隆產生的抗體稱之為多克隆抗體。
多克隆抗體作為一種重要工具被廣泛應用于科學研究和診斷中,它們能夠識別特定的抗原物質,可以應用于Western blot、放射性免疫測定、ELISA、直接-間接熒光抗體檢測、紅細胞凝集試驗、免疫組化(IHC)、免疫沉淀(IP)、免疫擴散、親和層析、酶學、基因分離等眾多實驗中。用途極其廣泛。
高親和性多克隆抗體能夠同時識別抗原上的多個表位,通過多價結合的協同效應大幅提升抗原抗體復合物的穩定性。這種特性在Western Blot(WB)和ELISA等實驗中尤為關鍵,多表位結合能夠有效放大信號并減少漏檢的風險,親和性低的抗體會因結合能力弱而導致信號捕獲不足而出現假陰性的結果。而且高親和性抗體對靶蛋白的微小結構變化(如糖基化、部分變性)具有更高容忍度,在免疫組化(IHC)等實驗中對構象變化的抗原仍能穩定結合,低親和性抗體對表位構象敏感,抗原輕微改變即可導致結合失效。多克隆抗體的高親和性是其核心優勢,是保障檢測靈敏度和實驗穩定性的基石,穩固的結合能力不僅能夠提升低豐度靶標的檢出率,還賦予了實驗體系更強的抗干擾能力
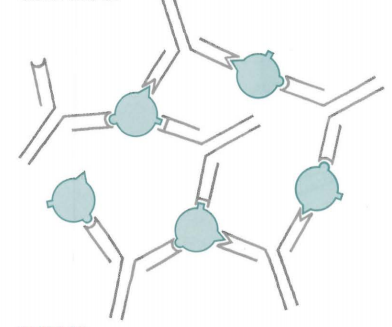
多克隆抗體與多價抗原結合
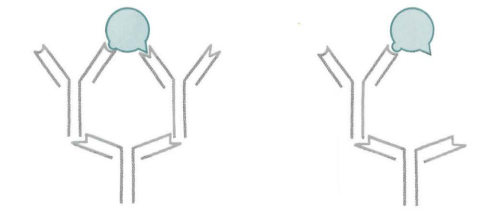 低親和力 高親和力
低親和力 高親和力
三、動物選擇
實驗動物選擇是制備多克隆抗體制備是否能達到預期的關鍵因素之一,廣泛的脊椎動物物種可用于生產抗血清,如:兔子、小鼠、羊、馬、驢、豬等。其中兔子是常規生產多克隆血清的一個很好的選擇。動物的選擇主要根據抗原的生物學特性和所需獲得抗體的數量和用途,如制備抗γ-免疫球蛋白抗血清,多用兔子和山羊,因動物反應良好,且能夠提供足夠數量的血清。
抗原與動物種屬之間的關系一般認為抗原的來源與免疫動物的親緣關系越遠,免疫原性越強,產生抗體的效價越高。而同種系或親緣關系較近者,產生抗體的效價低,甚至不產生抗體。比如:針對小鼠抗原的抗體反應可能在小鼠或大鼠中不發揮作用,但是在兔中就可以。免疫親緣關系較遠的哺乳動物可產生高達10mg/mL的抗體,但如果免疫同種異型動物,產生的抗體量低于1mg/mL,雞經常被用來制備IgY(等同于哺乳動物的IgG)的多克隆抗體,而且IgY不會和哺乳動物IgG發生交叉反應。
1. 小鼠:小鼠是嚙齒目中體型較小的動物。新生小鼠1.5g左右,21天斷乳時12~
15g,1.5至2月齡體重達20g以上,可供實驗使用。
2. 兔:兔耳大,表面分布有清晰的血管。有特殊的血清型和唾液型,血清型分為α'、β'、α'β'和 O 型四種。由于抗原刺激機體后,體液免疫應答反應強烈,所以兔被廣泛用于制備高效價的特異性強的免疫血清。應選擇年齡在6個月以上,體重以2~3kg為宜。

3.  羊:可用于生產多種抗血清,優先選擇成年個體(免疫系統成熟),健康狀態良好的羊。
羊:可用于生產多種抗血清,優先選擇成年個體(免疫系統成熟),健康狀態良好的羊。
4. 豚鼠:選擇成年(3個月以上)且健康的豚鼠(體重200-250g),此時免疫系統成熟,免疫后產生的抗體效價較高。?

四、抗原選擇
能被特異性免疫應答所識別的分子被稱為抗原。然而,不是所有的抗原都是免疫原。免疫原是指能引起體液免疫和(或)細胞免疫的分子。如大多數蛋白質、細菌、病毒等。分子量大于5KDa的抗原更易于刺激抗體產生,一些小分子物質(半抗原)如小的多肽、多糖、類脂和某些藥物等,只有在和有活性的大分子物質(載體,如BSA、OVA)偶聯時才能引起免疫應答。能引起抗體應答的抗原必定是免疫原。自然界中的抗原物質種類繁多,包括各種天然抗原、人工抗原、合成抗原、基因工程抗原等,絕大多數的天然抗原不是單一成分,在制備抗體時需要進行純化。一般而言,大多數動物的免疫系統是非常敏感的,用于免疫的抗原建議是純化品,抗原經12.5%的PAGE電泳后,僅出現一條區帶,即認為可作為免疫用抗原。
不同動物種類對同一抗原有不同的免疫應答表現,因此對不同性質的抗原選用的動物也不相同。蛋白質抗原一般適用于大多數動物,常用的有兔和羊,但在某些動物體內因為有類似物質或其他的原因,蛋白質抗原對這些動物免疫原性極差,如兔子對胰島素、綿羊對IgE、山羊對多種酶類均不易產生抗體。甾體激素多選用兔,酶多選用豚鼠。
五、佐劑應用
免疫佐劑是指預先或與抗原同時注入體內,可增強機體對抗原的免疫應答或改變免疫應答類型的非特異性免疫增強性物質,其目的是為了提高抗原對機體的免疫原性,提高機體產生抗體的效價。與僅使用抗原相比,其抗體的產量會更大。油性免疫佐劑介導的放大效應包括:(1)一種免疫原的倉庫,使其能在較長時間內緩慢釋放從而向免疫系統提呈;(2)免疫刺激被優化,一般免疫刺激劑和抗原集中于同一微環境中,并同時與抗原提呈細胞和淋巴細胞相互作用;(3)免疫系統細胞非特異性活化,而這種活化對產生抗體的反應有益。
目前動物免疫中應用廣泛的是弗氏佐劑和其它的一些油性佐劑,如:弗氏不完全免疫佐劑(加強型)、弗氏完全免疫佐劑(加強型)、乳化型快速完全免疫佐劑和乳化型快速不完全佐劑等,完全佐劑由不完全佐劑加卡介苗組成。由于都是油劑,因此在免疫動物時,建議先將佐劑與抗原按合適的體積比混勻,制成油包水型乳化液。初次免疫一般用完全佐劑,刺激機體產生較強的免疫應答;再次免疫時,使用不完全佐劑。弗氏不完全免疫佐劑(加強型)、弗氏完全免疫佐劑(加強型),乳化型快速完全免疫佐劑和乳化型快速不完全佐劑,是商品化的高效的佐劑之一。特別適合單抗研發用小鼠的免疫以及兔子、山羊、豚鼠等多克隆抗血清的制備。

在免疫動物前,應先將弗氏不完全免疫佐劑(加強型)、弗氏完全免疫佐劑(加強型)、乳化型快速完全免疫佐劑或乳化型快速不完全佐劑等油性佐劑與抗原按一定比例混合,制備成“油包水”乳狀液。可溶性抗原和免疫佐劑在乳化過程中,含有抗原的小水滴被油所捕獲,在非常黏的乳劑中形成顆粒,傳統的乳化方法有研磨法、注射器混合法、超聲法。這些方法抗原損耗大、用時長且不易操作。可以用手持移液器式佐劑乳化器進行乳化,乳化過程操作簡單、方便快捷、安全性高、用時少,幾分鐘就可乳化完全,且抗原幾乎無損耗。乳化器如下圖:

 乳化器乳化具體操作方法有2種:(1)將佐劑先加入乳化管,然后加少部分抗原攪拌乳化幾下后再加抗原繼續乳化,直到抗原加完再乳化幾分鐘即可。(2)抗原和佐劑加入乳化管,稍等抗原會沉入底部和佐劑分層,用攪拌器自上而下慢慢攪拌佐劑入抗原層,慢慢下移這時會發現混合液很快乳白越來越粘,幾分鐘就可完成。乳化示意圖如下:
乳化器乳化具體操作方法有2種:(1)將佐劑先加入乳化管,然后加少部分抗原攪拌乳化幾下后再加抗原繼續乳化,直到抗原加完再乳化幾分鐘即可。(2)抗原和佐劑加入乳化管,稍等抗原會沉入底部和佐劑分層,用攪拌器自上而下慢慢攪拌佐劑入抗原層,慢慢下移這時會發現混合液很快乳白越來越粘,幾分鐘就可完成。乳化示意圖如下:
乳化完成后,將一滴乳劑滴入水中,若保持完整不分散,成滴狀浮于水面,則為乳化完全,為合格的油包水劑。各成分在乳化后不會分散,在運用到宿主組織后,才能發揮抗原倉庫的作用。如下圖:

弗氏不完全免疫佐劑(加強型)、弗氏完全免疫佐劑(加強型)、乳化型快速完全免疫佐劑和乳化型快速不完全佐劑的使用比例是30~50%。接近30%乳化粘度增加,接近50%乳化粘度減小。因此建議夏季使用低濃度冬季使用高濃度乳化,這樣既能得到很好的免疫效果也能減少注射時帶來的阻力困難。
六、免疫動物
1. 免疫劑量
一般而言,需要納克到微克級的抗原加上佐劑才能誘導高滴度的抗體反應,例如,兔需要免疫500~1000μg,小鼠需要10~200μg,山羊或者綿羊需要250~5000μg可溶性抗原加上乳化型快速完全免疫佐劑能誘發高滴度的抗體反應。越小的動物需要的抗原/佐劑混合物的濃度越低,但是產生抗體所需的抗原劑量并不一定必須要根據動物的大小而增加或減少。可能一只4kg的兔需要的抗原劑量同25g小鼠所需的一樣。抗原的劑量非常關鍵,高劑量的抗原導致低親和力的B細胞活化,而低劑量抗原能引起高親和力的B細胞活化。佐劑的應用使低劑量抗原進行免疫成為可能,佐劑能提高抗體滴度,并能減少免疫耐受產生的機會。
2. 免疫途徑
抗原的進入途徑決定了抗原吸收、分布和代謝的速度,吸收越快,分解代謝越快,對機體的影響時間越短。吸收越快,單位時間內的有效抗原量就越大,機體的免疫應答就越強,不良反應也越強。應根據不同抗原及實驗要求選擇不同的免疫途徑。免疫途徑包括皮內注射、皮下注射、淋巴結內注射、腹腔注射、靜脈注射、肌內注射及脾內注射等途徑。可溶性抗原(糖蛋白、脂蛋白、酶類、補體、細菌外毒素、多糖和核酸等)及抗原量少的情況下,一般多采用添加免疫佐劑,如完全免疫佐劑和不完全佐劑,在淋巴結內或淋巴結周圍或足墊、皮內、皮下多點注射的方式;顆粒性抗原(各種動物細胞抗原、細菌抗原和寄生蟲抗原等)及抗原量多的情況下,可不添加佐劑,直接采用靜脈、腹腔、肌內注射的方式。也可以根據具體情況,聯合不同的免疫途徑制備高效價抗體。
3. 免疫方法(以兔子為例)
(1) 皮下注射:
從靠近頸部后側的一側開始,用拇指和食指捏住皮膚。將皮膚從身體上拉開,將針插入已形成的空隙中。將針的末端從一側向另一側移動一小段距離,以確保它不會插入肌肉或身體壁。按下活塞以注射所需的量。暫停幾秒鐘。當針頭被拔出時,應用食指和拇指輕輕按壓注射部位,防止接種液外滲。如下圖:
(2)肌內注射
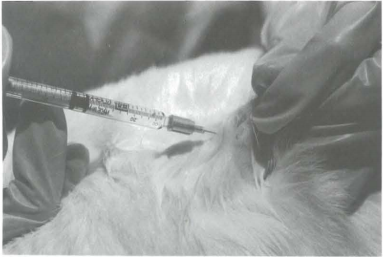
將兔子從籠子里取出,放在足夠粗糙的鋼絲或固體表面上,讓兔子感到舒適。應避免讓兔子置于光滑的表面上,因為兔子會在任何光滑的表面上收縮肌肉。
注射通常在后腿的大腿肌肉中進行。從前部抓住腿,將注射器插入大腿肌肉靠近髖部的后部。將針插入肌肉,輕輕嘗試抽回活塞。如果遇到阻力,可以繼續進行注射。如果出現血液,說明針頭誤入腿上的小靜脈或動脈。拔出注射器,移動到附近的部位并再次嘗試。抗原應緩慢、平穩地注入。注射完成后拔出針頭,輕輕按摩注射部位。如下圖:
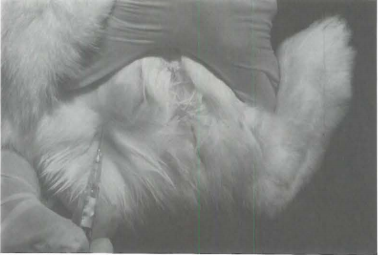
(3)皮內注射
皮內注射在較大動物的免疫接種中相當常見。與肌內注射一樣,皮內注射用于以非常緩慢的速度釋放免疫原。接種物被注射在皮膚層之間,并緩慢吸收進入體內。
注射部位可選擇脅部高位(肋骨與髖骨之間)或背部區域。剃除適當大小的區域以露出皮膚,用食指和拇指夾住皮膚,確認針頭與注射器連接緊密。針頭斜面朝上,輕微刺入皮下后繼續在皮層間平行推進至少0.5~0.7厘米。接種液應在皮下形成致密性皰疹,拔針時用指腹壓閉針道,




 豫公網安備 41031102000387號
豫公網安備 41031102000387號